· 化学 Fe2と1,10フェナントロリンにより錯体を形成させて吸光度を測定する際に,30分・60分・90分と時間を置いているのですが,机の上に出しておく(蛍光灯とか日光にあたってοフェナントロリン鉄の錯体を用いるアルミニウムーバナジウム合金中の鉄の吸光光度定量法について検討したバナジウムを含む酸性溶液に塩酸ヒドロキシルアミンを加えて還元するとともに錯体を生成させ,酢酸ナトリウムと水酸化ナトリウムを用いて phを 40 ~ 45 とすることにより無色と1,10フェナントロリンの鉄 錯体はフェロイン (ferroin) と呼ばれ、電位の酸化還元指示薬(標準酸化還元電位 E 0 = 106 V) として滴定分析、吸光光度分析に用いられる試薬である。 合成 フェナントロリンは、スクラウプ反応で合成することができる。
質問箱
1 10-フェナントロリン 鉄 錯体 ph
1 10-フェナントロリン 鉄 錯体 ph-1,10‐フェナントロリンとFe2、第一鉄トリス(‐フェナントロ リン)鉄(II)またはFe(phen) 32によって形成される錯体は明 るいオレンジ色です。錯体の構造の3Dモデルを図2に示します。 鉄は、 Fe2(第一鉄イオン)の形態に加えて、3(第二鉄イ鉄(II),1,10フェナントロリン及びテトラヨードフルオレセインから成る三元錯体の溶媒抽出 並列タイトル (alternative) Solvent extraction of the ternary complex composed of iorn (II), 1, 10phenanthroline, and tetraiodofluorescein 著者 (creator) 星,座




Images Of 1 10 フェナントロリン Japaneseclass Jp
タイトル 1,10フェナントロリンを用いる鉄の比色定量におけるpH調節と鉄の状態について 著者 立花 啓助 出版地(国名コード) JP 出版年 (W3CDTF) NDLC1,10フェナントロリン鉄(ii)硫 酸塩 17 塩化水素 0 1215 水 97 注記:これらの値は、製品規格値ではありません。 危険有害成分 安衛法「表示すべき有害物」該当成分 塩化水素、1,10フェナントロリン鉄(ii)硫酸塩フェナントロリンの性質の一部は2,2'ビピリジン(英語版)と似ている。 1,10フェナントロリンの鉄(II) 錯体はフェロイン (ferroin) と呼ばれ、電位の酸化還元指示薬(標準酸化還元電位 E0 = 106 V) として滴定分析、吸光光度分析に用いられる試薬である。
この鉄(ii)と鉄(iii)に対する選択性を用いて試料中の鉄(ii)と鉄(iii)の比率を求めることもできる。 *3 1,10フェナントロリンは酸性条件では酸型になり鉄と錯体を作らなくなるので、phの設定(ph 3~9)には注意が必要である。衝液添加の前に行う理由は、還元を速やかに行うためである。pH を調整後、緩衝液025 mL を添加し、水を加えて全量5 mL とする。攪拌して30 分放置した後、510 nm で吸光 度を測定する。 ・溶存Fe(Fe2、Fe3)の測定Coordination complex Chemical class 0000 claims abstract description 12;
床で使用されている.ブレオマイシンは,体内の鉄イオンと反応して鉄錯体を形成し,鉄周辺で活性酸 素種をつくり,DNA を切断すると考えられている.ブレオマイシン錯体のFe2とO 2 との相互作用は, ヘモグロビン中のFe2とO 2 との相互作用と類似点がみられる.鉄イオン は,3分子の1,10フェナントロリンと錯体を形成する。配位結合は1,10フェナントロリンの2個の 窒素との間で生じる。この時の鉄イオンは,d2sp3浬成軌道による正八面体構造(双四角錐型,双ピラ ミッド型)の配位をする。Binding Effects 0000 title claims abstract description 24;




希土類錯体を用いた高耐久型波長変換フィルムに関する研究 Pdf 無料ダウンロード




15 3085号 光電変換特性を有するジピリン金属錯体シート及びその製造方法 Astamuse
この実験は、鉄(Ⅱ)イオンFe2+が1,10 -フェナントロリンと反応して、 Fe2+:phen=1:3の金属キレートを生成する反応を利用している。 この金属錯体は長時間変化せず安定で、1,10 -フェナントロリンと錯体を形成するのは 2価の鉄のみである。合成 硫酸鉄 (II) と1,10フェナントロリンを水溶液中で反応させることによって調製できる。 3 phen Fe 2 Fe ( phen ) 3 2 {\displaystyle {\ce {3 {\mathit {phen}}\ Fe^ {2}>\ Fe ( {\mathit {phen}})3^ {2}}}} 鉄は低スピンの電子配置をとり、D 3 対称の八面体配位をとっている。 フェロイン錯体の特徴的な色は、金属イオンと配位子の間の 電荷移動遷移 に起因する。1,10フェナントロリンを用いる鉄の比色定量におけるpH調節と鉄の状態について 1) F J Welcher "Organic Analytical Reagents", Vol III, p (1948), (D Van Nostrand Company, Inc, New York) E B Sandell "Colorimetric Determination of Traces of Metals", 3rd Ed, p 540 (1959), (Interscience Publishers, Inc, New York)




Jpa 希土類金属の抽出剤及び抽出分離法 Google Patents




化学に詳しい方おねがいします 画像の構造式がテストで出たのですが なん Okwave
PH 図 鉄(ⅠⅠ)・1,10-フェナントロリン錯体の吸光度 に対するpHの影響 甘:鉄(ⅠⅠトバナジウムーフェナントロリン系 骨:鉄(ⅠⅠトフェナントロリン系 4-4 鉄(ⅠⅠ)・1,10-フェナントロリン錯体生成のpH1,10phenanthrolines Chemical class 0000 title claims abstract description 77;チオシアナト鉄(iii)錯体、1,10フェナントロリン鉄(ii)錯体および銅(i)錯体などはこの例で、前者では から へ電子が移動して 基と を生成し、後者では金属の 電子が配位子の 軌道へ移動します。




Jpa 希土類金属の抽出剤及び抽出分離法 Google Patents




至急お願いいたします 化学 画像の物質は1 10 フェナントロリン錯体の Okwave
三元錯体(ternary complex)の生成を利用する方法は、この欠点をある程度解決するので、増感法としてよく用いられます。 例えば、銀、1,10フェナントロリン(phen)、ブロモピロガロールレッド(BPR)より成る錯体では、一次錯体の 分子がさらに とイオン会合して を生成し、 はで選択性Ligands Substances 0000 title claims abstract description 24;Discuss1 1,10phenanthroline metal complex Chemical class 0000 title claims description 28;




10 号 金属錯体を含む炭素ナノチューブ分散剤 Astamuse




16 号 酸素還元触媒 Astamuse
Oフェナントロリン鉄錯体は陰イオン対として有機溶媒に抽出されることより、陰イオンの間接的定量に用いられる。また、近年は有機合成法の触媒として知られるルテニウム錯体の配位子にも用いられる。 1水塩は融点 98~100℃、無水物は融点 117℃である。 · Fe2と1,10フェナントロリンにより錯体を形成させて吸光度を測定する際 鉄をフェナントロリンで定量する際、pHを3.5にする理由を教え アルミニウム箔中の鉄の定量と言う実験の中で1,10フェナントロリンを用いて鉄を錯体にし鉄 (Ⅱ)、鉄 (Ⅲ)はともにこれら配位子の3分子と結合してトリス(tris)錯体を生成する。 すなわち下記の二つである。 Fe (phen) 3 2 (tris (1,10phen)iron (Ⅱ)) Fe (phen) 3 3 鉄 (Ⅱ)をferro、鉄 (Ⅲ)をferriというので、これと1,10phenanthrolineの語尾のineからeを取って、ferroin(フェロイン)およびferriin(フェリイン)とよぶ。 広義にはN=CC=N型の配位基をフェロインferroineと



Blogjpmbaheqynf 最新 フェナントロリン 鉄 錯体 2240 フェナントロリン 鉄 錯体 化学式



3回生実験のこと 光吸収 1 2
Membrane Substances 0000 title abstract 4;鉄不純物濃度の異なるめっき液を作成し, めっき液を城東 式簡易分析器専用のセルにマイクロピペットで01mL採取 し, 塩酸(11)を一滴加える。次に, 塩酸ヒドロキシルアミン(10%)を 5mL 加え振り混ぜたのちに1, 10 -フェナントロリン溶液(02%)を2.1,10フェナントロリン塩酸塩を用いて,溶液を調製 最終濃度が 4x10−4 M になるように,メスフラスコに採取 3.CH 3 COOH-CH 3 COONa を用いて,pH~5 の緩衝溶液を調製 最終濃度が 01 M になるように,メスフラスコに採取 4.510 nm で吸光度測定 試料の測定




Images Of 1 10 フェナントロリン Japaneseclass Jp




非線形化学反応 一般財団法人宇宙システム開発利用推進機構
そこで次に,よく知られている1,10 Phenanthroline(oフェナントロリン,または ophen)を配位子として過剰量添加する方法につい て検討した。 3.oフェナントロリンを添加する方法の検討 鉄(II)イオンとoフェナントロリンの1:3錯体鉄 541 要旨 試料を水に溶かし,塩酸で微酸性とした後,溶液中の鉄を塩酸ヒドロキシルアミンで還元し, 1, 10フェナントロリン及び酢酸アンモニウムを加えて生成する1, 10フェナントロリン鉄錯体の吸光度を 測定して鉄を求める。 542タイトル: 特許公報(b2)_鉄の定量方法 出願番号: 年次: 11 ipc分類: g01n 31/00,g01n 31/22,g01n 21/78



質問箱




Pdf Fundamental Knowledge Of Chemical Analysis Spectrophotometry
フェムト秒発光分光による銅(I)フェナントロリン錯体の 光誘起擬ヤーン・テラー構造変化の実時間観測: 置換基による構造制御とその超高速ダイナミクスへの影響 岩村宗高、竹内佐年、田原太平 背景と目的 Cu(dmphen)2 (dmphen = 2,9dimethyl 1,10phenanthroline)低配位錯体 一配位錯体(極めて稀) 二配位錯体 Cu(I), Ag(I), Au(I), Hg(II) (Pd(0), Pt(0)) d10 三配位錯体 Cu(I), Ag(I), Au(I), Hg(II) (Pd(0), Pt(0)) d10 CuCl 2, Ag(NH 3) 2 , Au(CN) 2AuClL (L = PR 3, R 2S), Au(PR 3) 2 Hg(CN) 2, Hg(CH 3) 2 N M N N Me 3Si SiMe SiMe3 SiMe3 SiMe3 Me3Si M = Fe(III), (Sc(III), Y(III) Cu(CN) 2, Ag(PPh 3) 3応{式( 1 )}が,pH 4~6 付近で 1,10 フェナントロリン (phen)の共存によって熱力学的に有利に進行することをポテ ンショメトリーで示した8)。 2RSH+2Fe(phen)33+ RS SR+2Fe(phen)32++2H+( 1 ) このことは,式( 2 )のネルンスト式からも明らかである。
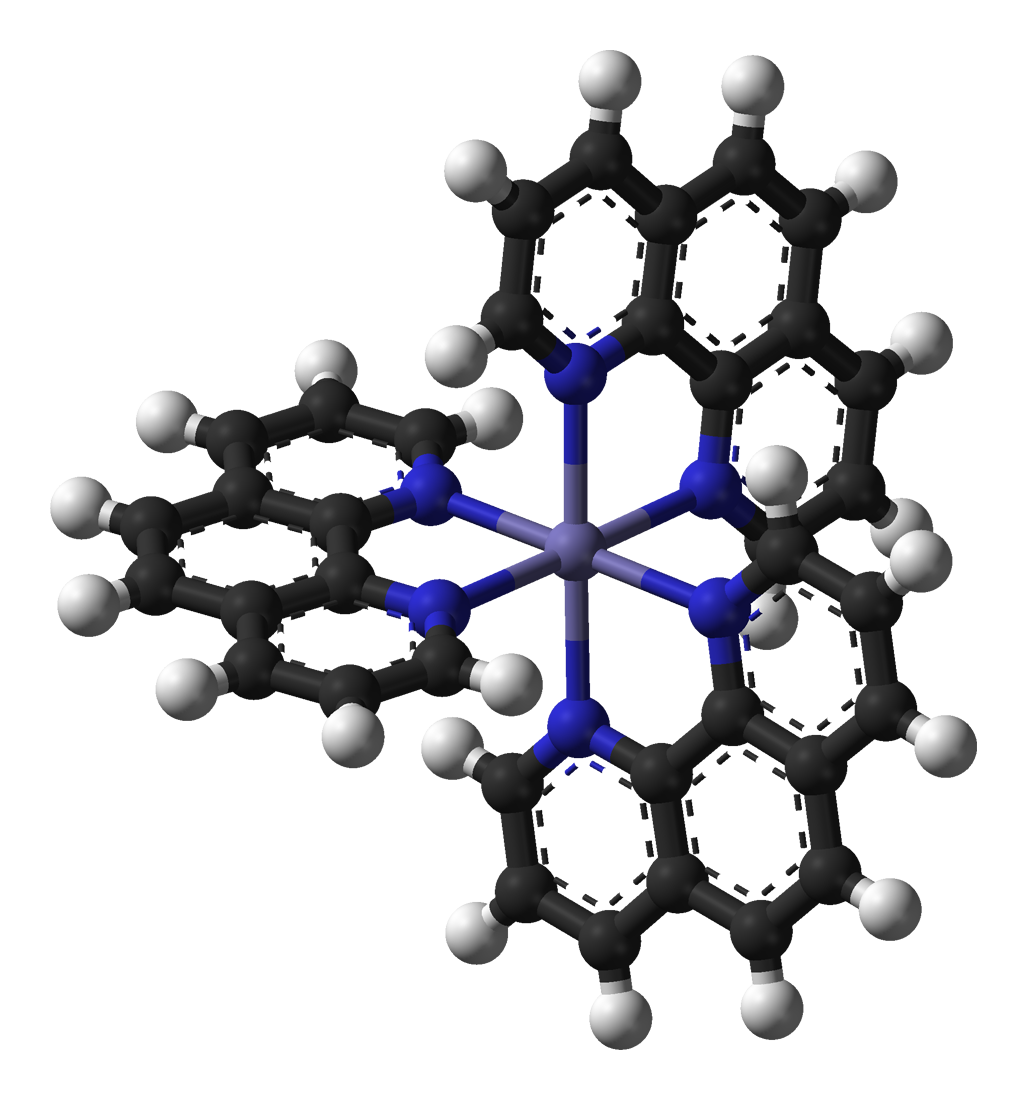



フェロイン Wikipedia




10 号 有機金属錯体 3次元構造体 およびそれらの製造方法 Astamuse
析法の感度の限界はほぼ105~10一6"で あるといって もさしつかえない5)。 さて,phenは 水溶液中で鉄(II)と31の モル比で 反応し,赤とう色の金属キレート陽イオンFe(phen)3P を生成し,図1に 示すように510mμ に吸収極大があManufacturing process Methods 0000 title claims description 5; · 概要)ph緩衝液の影響や効果を中心に Fe(Ⅱ)とフェナントロリンの錯体形成は、ph=45で行う必要があります。 そのため、酢酸アンモニウムを緩衝剤としてphをコントロールし適切な条件で発色させます。




エチレンジアミン四酢酸 Edta の性質とキレート滴定について解説 ジグザグ科学 Com



マイクロアッセイ Uibc 不飽和鉄結合能 キット バソフェナントロリン法 Metallogenics
Polymerization reaction Methods 0000 claims abstract description 24;1,10フェナントロリン textskipToContent textskipToNavigation お客様のニーズに合ったより良いサービスを提供するために、当ウェブサイトではCookieを使用しています。1 Fe(II)イオンの吸光係数について 2 鉄(II)フェナントロリン錯体 3 モル濃度9819×10^2の塩酸とモル濃度9819×10^3の炭酸ナトリウムの中和点のpHを 4 化合物のモル吸光係数データベースを教えて下さい 5 モル吸光度係数の値・・・。




Analytical Chemistry 応用理数 化学講座



公表特許公報



H28 1班 世にも奇妙な 振動反応 ここなっつぱいん




Pdf Electrochromism Of Coordinated Metal Complex




フェナントロリン Wikipedia



特許 知財ポータル Ip Force




Jpa 希土類金属の抽出剤及び抽出分離法 Google Patents



H24 6班 ハッ 振動反応



Bu 4n 2 Zn Dmit 2 と 1 3 ジブロモプロパンを反応させて合成した 収率 98 この反応では 反応温度と反応溶液の濃度を調整することがポイントである 次いで チオン体 1 とオキソン体 2a B 3 の Meo 3p クロスカップリング反応により Tdd Pdf Free Download



公表特許公報




Woa1 過酸化水素製造方法 過酸化水素製造用キットおよび燃料電池 Google Patents



0 件のコメント:
コメントを投稿